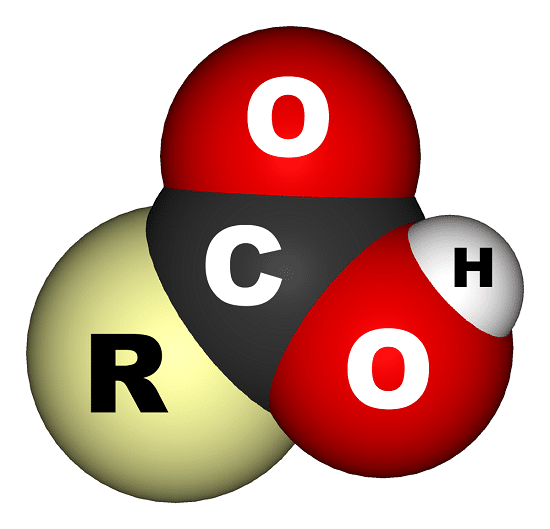
Son sustancias o compuestos orgánicos utilizados en procesos químicos e industriales que provienen naturalmente de las grasas, aceites vegetales, lácteos y frutos cítricos. Una de sus principales características es que están formados por átomos unidos por enlaces covalentes carbono – carbono que al unirse al hidrógeno, nitrógeno u oxígeno forman otros compuestos.
Estos compuestos tienen propiedades ácidas, además de que sus dos átomos de oxígeno son electronegativos y suelen atraer los electrones del átomo de hidrógeno del grupo hidroxilo, debilitando el enlace y produciendo en ciertas condiciones lo que se conoce con el nombre de ruptura heterolítica.
Clasificación de los ácidos carboxílicos
Se les clasifica de acuerdo a la cantidad de grupos carboxilos que posea cada átomo y pueden ser:
- Monocarboxílicos: una molécula contiene un grupo de carboxilo (fórmico, acético, palmítico, esteárico y valérico).
- Dicarboxílicos: cada átomo posee dos grupos carboxilos (oxálico, malónico, glutárico, adípico, pimélico, subérico y sebácico).
- Tricarboxílico o policarboxílico: en una misma particula hay tres grupos carboxilos (cítrico, aconitico, tricarbalitico).
Dentro del grupo de los ácidos carboxilos, se les categoriza de acuerdo a la cantidad de átomos de carbono que los conforman y por ejemplo, en la solución química del ácido acético, se afirma que éste es el segundo de los carboxílicos, después del fórmico o metanoico, que solo tienen un carbono y antes del propanoico que posee una cadena de tres carbonos
Propiedades de los ácidos carboxílicos
- Forma molecular: de tipo trigonal plana.
- Estado: principalmente sólido y con más de ocho átomos, al menos de que posean doble enlace.
- Solubilidad: a mayor cantidad de carbono menos solubles en agua. Al pasar los diez átomos de carbonos son insolubles en agua pero más solubles en el alcohol por los enlaces de hidrógeno que posee.
- Olor: característicamente ácido pero a mayor cantidad de carbonos más tenue se vuelve.
- Punto de ebullición superior al de los alcoholes, cetonas y aldehídos.
- De su aleación con hidruro de litio y aluminio resultan alcoholes primarios.